Российские исследователи успешно создали улучшенную модель химического поражения роговицы у лабораторных мышей. Предполагается, что это новаторское достижение позволит разработать более эффективные методы лечения химических ожогов глаз у людей, тем самым предотвращая слепоту. Об этом сообщили представители Российского научного фонда (РНФ).
Химические ожоги роговицы представляют собой одну из наиболее серьезных проблем в офтальмологии. Они часто приводят к необратимым повреждениям, значительной потере зрения, образованию плотных непрозрачных рубцов и аномальному прорастанию кровеносных сосудов в роговицу. Существующие на сегодняшний день методы лечения, включающие противовоспалительные препараты или средства, предотвращающие рубцевание, зачастую показывают недостаточную эффективность и могут вызывать нежелательные побочные реакции. В крайне тяжелых случаях единственным решением остается трансплантация роговицы, но даже эта процедура не всегда гарантирует успех, поскольку возможны отторжение или помутнение пересаженного трансплантата.
По словам авторов исследования, разработка действенных терапевтических подходов затруднена из-за высокой погрешности существующих моделей химического ожога (около 40%), использующих нанесение щелочи или кислоты на глаза лабораторных животных.
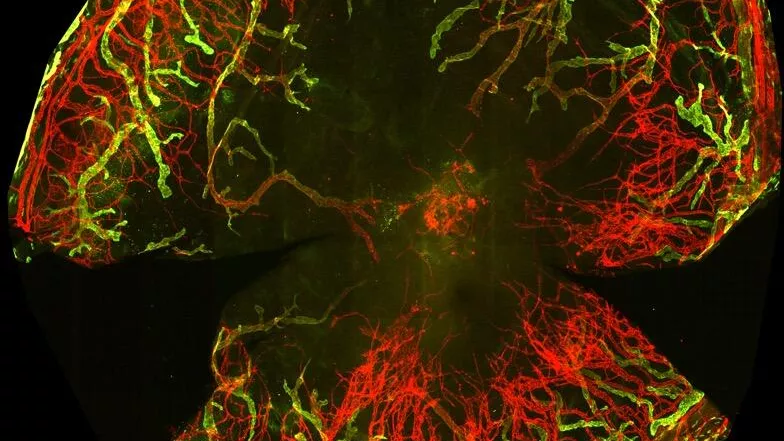
Микрофотография сосудов в роговице (© Фото предоставлено пресс-службой МГУ)
Ученые из Московского государственного университета имени М.В. Ломоносова существенно усовершенствовали модель химического ожога роговицы у мышей, оптимизировав экспериментальную методику и значительно снизив погрешность измерений. В ходе эксперимента использовались растворы гидроксида натрия (щелочи) с различными концентрациями для достижения различных сценариев заживления роговицы. Предполагалось, что низкая концентрация щелочи будет способствовать регенерации раны, тогда как высокая приведет к формированию рубца.
Благодаря новой модели, исследователям удалось глубоко изучить клеточные и молекулярные изменения в роговице глаз подопытных мышей. Было установлено, что при концентрации щелочи 20 граммов на литр количество миофибробластов – клеток, играющих двойную роль в заживлении (помогают затягивать раны, но также способствуют рубцеванию) – уменьшалось уже через неделю после травмы. К исходу третьей недели эти клетки полностью исчезали, что коррелировало с полным восстановлением прозрачности роговицы.
Руководитель проекта Павел Макаревич за работой (© Фото предоставлено пресс-службой МГУ)
В случае использования щелочи с концентрацией 40 граммов на литр, миофибробласты сохранялись даже по прошествии 21 дня, включая их присутствие во внутреннем слое роговицы – эндотелии, что приводило к ее помутнению. Высокая концентрация гидроксида натрия также спровоцировала быстрое врастание кровеносных и лимфатических сосудов в толщу роговицы. Уже к седьмому дню эксперимента эти сосуды начинали покрываться гладкомышечными клетками, что способствовало их стабилизации и окончательной потере прозрачности роговицы.
Полученные результаты имеют огромное значение как для фундаментальных исследований, так и для клинической практики в медицине. Они значительно расширяют понимание механизмов естественного восстановления роговицы после различных травм, открывают новые возможности для тестирования препаратов, направленных на предотвращение ее рубцевания, а также прокладывают пути для создания методов, способствующих ускоренной регенерации клеток роговицы.
Павел Макаревич, руководитель данного проекта, поддержанного грантом РНФ, заведующий лабораторией медицинской биоинженерии Центра регенеративной медицины и доцент кафедры биохимии и регенеративной биомедимедицины факультета фундаментальной медицины МГУ, подчеркнул: «Мы убеждены, что наша модель станет незаменимым инструментом для разработки принципиально новых подходов к лечению повреждений роговицы. Ключевым открытием стала демонстрация решающей роли миофибробластов в процессе заживления. Мы четко показали, что именно скорость их исчезновения определяет, восстановится ли роговица до состояния прозрачности или же на ней образуется рубец. В ближайшем будущем мы планируем использовать эту усовершенствованную модель для идентификации источников миофибробластов и выяснения того, какие молекулярные и клеточные факторы регулируют различные исходы заживления при повреждениях различной степени тяжести.»